
Sicherheit und Wirksamkeit der Kombination von 308 nm monochromatischem Excimerlicht und topischer 0,1% -Tacrolimus-Salbe bei segmentaler Vitiligo: Eine offene Studie
von SWAPNIL SHAH, MD; JAGADISH SAKHIYA, MD; PRANOTI DESHPANDE, MD; DHRUV SAKHIYA, MBBS; und ARUN C. INAMADAR, MD
Die Ärzte Shah, Sakhiya, Deshpande, Sakhiya und Inamadar sind im Ashwini Rural Medical College Hospital and Research Center Solapur in Maharashtra, Indien, tätig.
J Clin Aesthet Dermatol. 2020;13(2):xx–xx
Zusammenfassung
HINTERGRUND: Vitiligo ist eine erworbene Erkrankung, die durch depigmentierte Makula oder Flecken auf der Haut aufgrund des Verlusts funktioneller Melanozyten gekennzeichnet ist. Segmentale Vitiligo (SV) ist ein therapieresistenter Subtyp von Vitiligo.
ZIEL: Wir untersuchten die Sicherheit und Wirksamkeit von 308 nm monochromatischem Excimerlicht (MEL) in Kombination mit 0,1% iger Tacrolimussalbe zur Behandlung von SV.
METHODEN: Fünfzig Patienten mit SV wurden aufgenommen. MEL wurde an wechselnden Terminen in Kombination mit topischem Tacrolimus verabreicht. Klinische Fotos wurden einmal im Monat gemacht. Zwei unabhängige Dermatologen analysierten und bewerteten die Ergebnisse.
ERGEBNISSE: Fünf Patienten mussten nachuntersucht werden. Was den Behandlungserfolg insgesamt anbelangt, so wiesen 77,8 Prozent der Patienten eine Repigmentierung von mindestens 75 Prozent auf. Insbesondere wiesen 35,6 Prozent der Patienten eine vollständige (100%) Repigmentierung auf (Grad 5), wohingegen 42,2 Prozent der Patienten eine Repigmentierung von mehr als 75 Prozent aufwiesen (Grad 4).
FAZIT: Die Kombinationstherapie mit topischem 0,1% Tacrolimus und einer 308-nm-Excimer-Lampe scheint wirksam zu sein und ein gutes Sicherheitsprofil zu haben. Die Dauer der Erkrankung war ein statistisch signifikanter Faktor, der umgekehrt mit der Behandlungserfolgsrate korrelierte. Der Ort der Vitiligo spielt ebenfalls eine wichtige Rolle beim Behandlungsergebnis, da Gesichtsläsionen am besten auf die Behandlung ansprachen.
STICHWÖRTER: Monochromatisches Excimerlicht, Hautpigmentierung, Tacrolimus, Vitiligo
Vitiligo ist eine erworbene Pigmentstörung, die durch depigmentierte Makula oder Flecken auf der Haut aufgrund des Verlusts funktioneller Melanozyten gekennzeichnet ist. Sie betrifft rund 0,5 Prozent der Weltbevölkerung.1 Vitiligo wird entweder als fokal, generalisiert oder segmental eingestuft. Während verschiedene Behandlungen, wie topische Steroide, topische Calcineurin-Inhibitoren, Psoralen-Ultraviolett A und Schmalband-Ultraviolett B, bei der Repigmentierung von fokaler und generalisierter Vitiligo wirksam sind, ist ihre Wirksamkeit bei segmentaler Vitiligo (SV) eingeschränkter.2 SV ist in der Regel therapierefraktär und ein chirurgischer Eingriff ist eine bevorzugte Interventionsmethode.3 Obwohl eine Operation in den meisten Fällen zu einer zufriedenstellenden Repigmentierung führt, ist sie bei Kindern schwierig durchzuführen und geht häufig mit Komplikationen einher, darunter Farbabweichungen, Kopfsteinpflaster und Narbenbildung an der Spenderstelle.4
Der Excimer-Laser wurde bereits bei der Behandlung von Vitiligo, einschließlich SV, eingesetzt und kann Läsionen einzeln behandeln, wodurch die Übertragung höherer Fluenzen erleichtert und die umliegende normale Haut besser geschützt wird. Die alleinige Anwendung des Excimer-Lasers ist bei der Behandlung von SV nicht vorteilhaft.5 In neueren Berichten wurde jedoch gezeigt, dass es bei der Behandlung von SV in Kombination mit einem topischen Steroid oder topischen Calcineurin-Inhibitor wirksam ist.6—8
Topische Calcineurin-Inhibitoren, die durch Immunmodulation wirken, sind bei Vitiligo nützlich und fördern die Repigmentierung, ohne eine systemische Immunsuppression zu verursachen.9
Eine monochromatische 308-nm-Excimerlampe (MEL) hat einen ähnlichen Wirkmechanismus wie der 308-nm-Excimer-Laser.10 In dieser Studie untersuchten wir die Anwendung von MEL in Kombination mit einer topischen 0,1% -Tacrolimus-Salbe zur Behandlung von SV.
Materialien und Methoden
Diese Studie wurde in einer dermatologischen Klinik in Zentralindien durchgeführt. Die ethische Genehmigung wurde eingeholt und die Einwilligung nach Aufklärung und Foto der teilnehmenden Patienten eingeholt. Insgesamt 50 aufeinanderfolgende Patienten, bei denen SV klinisch diagnostiziert wurde, wurden in diese Studie aufgenommen. Fünf Patienten mussten jedoch nach einem Monat nicht mehr untersucht werden und wurden von der Studie ausgeschlossen. Von dieser Studie ausgeschlossen waren Patienten mit generalisierter Vitiligo, Patienten, die zuvor in den letzten drei Monaten mit irgendeiner Form von Phototherapie behandelt wurden, Patienten, bei denen in der Vergangenheit immunsuppressive oder photosensibilisierende Mittel eingenommen wurden, und Patienten, die sich einer Operation wegen Vitiligo unterzogen hatten.
Behandlung.
Nach Erteilung der Einverständniserklärung wurden alle Patienten mit Xenonchlorid 308 nm MEL (Exciplex; Clarteis, Antipolis, Frankreich) behandelt. Die mit diesem System verfügbare Spotgröße betrug 5 × 5 cm. Eine geeignete Silikonschablone der Größe SV wurde verwendet, um die umliegende Haut vor Verbrennungen zu schützen und eine periläsionale Hyperpigmentierung zu vermeiden. Die Behandlung wurde mit einer Fluenz von 100 mJ/cm2 begonnen und pro Sitzung um 50 mJ/cm2 erhöht, bis nach 24 Stunden ein leichtes Erythem auftrat. Wenn ein intensives Erythem länger als 48 Stunden bestand, wurde die nächste Sitzung übersprungen, bis das Erythem abgeklungen war und die Dosis um 100 mJ/cm2 reduziert wurde. Die reduzierte Dosis wurde für die folgenden zwei Sitzungen beibehalten und dann um 50 mJ/cm2 erhöht. Die Behandlung wurde 2- bis 3-mal pro Woche an nicht aufeinanderfolgenden Tagen verabreicht. Zusätzlich wurden die Patienten angewiesen, zweimal täglich eine 0,1% ige Tacrolimus-Salbe auf die betroffenen Stellen aufzutragen. Wenn der Patient nach 15 bis 20 MEL-Bestrahlungssitzungen keine Pigmentierung aufwies, wurde der Fall als Behandlungsversagen eingestuft. Darüber hinaus wurde die Behandlung abgebrochen, wenn nach dem ersten Ansprechen der Repigmentierung nach 10 bis 15 aufeinanderfolgenden Sitzungen kein Fortschreiten der Repigmentierung eintrat.
Zu Analysezwecken wurden einmal im Monat klinische Fotos aller Patienten aufgenommen, und zwei unabhängige Dermatologen bewerteten die Ergebnisse, indem sie diese Fotos überprüften. Die Repigmentierung wurde wie folgt eingestuft: Grad 0 (keine Repigmentierung), Grad 1 (1 bis 25% Repigmentierung), Grad 2 (25 bis 50% Repigmentierung), Grad 3 (50 bis 75% Repigmentierung), Grad 4 (75 bis 99% Repigmentierung) und Grad 5 (100% Repigmentierung).
Alle während des Behandlungszeitraums beobachteten Nebenwirkungen wurden ebenfalls aufgezeichnet.
Statistische Analyse.
Eine univariable und multivariable logistische Regression wurde unter Verwendung des Softwareprogramms Statistical Package for TheSocial Sciences Version 21 (IBM Corp., Armonk, New York) in einer Reihe durchgeführt, um die unabhängigen prognostischen Faktoren zu bestimmen, die mit dem Behandlungserfolg verbunden sind. Die Microsoft Excel 2007-Ausgabe (Microsoft Corp., Redmond, Washington) wurde zur Berechnung von Chancenverhältnissen (OR) und 95% -Konfidenzintervallen (CIs) verwendet.
Ergebnisse
Die demografischen Details der 45 SV-Patienten, die in der vorliegenden Studie analysiert wurden, sind in Tabelle 1 dargestellt. In unserer Studie waren die weiblichen Patienten den männlichen Patienten zahlenmäßig überlegen, und zwar mit einem Verhältnis von 2, 4:1. Das Durchschnittsalter beim Auftreten von SV betrug 18 Jahre, wobei der jüngste Proband drei Jahre und der älteste 60 Jahre alt war. Die durchschnittliche Krankheitsdauer betrug zum Zeitpunkt dieser Studie 16 Monate. Bei den meisten Patienten (n = 21/45; 46,6%) traten Vitiligo-Läsionen im Gesicht auf, gefolgt von sieben Patienten mit Läsionen an der Taille (15,6%) und sechs mit Läsionen am Hals (13,3%).

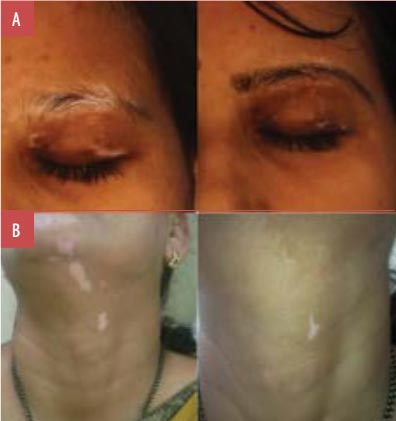
Unter Berücksichtigung des Behandlungserfolgs lag der Anteil der Patienten mit einer Repigmentierung von mindestens 75 Prozent an der Gesamtbevölkerung bei 77,8 Prozent (n=35). Unabhängig davon wiesen 35,6 Prozent (n=16) der Patienten eine 100-prozentige Repigmentierung auf (Grad 5) (Abbildungen 1—5), wohingegen 42,2 Prozent (n=19) der Patienten eine Repigmentierung von mehr als 75 Prozent aufwiesen (Grad 4) (Abbildungen 6—9). In der Zwischenzeit gaben 6,7 Prozent (n=3), 6,7 Prozent (n=3) und 2,2 Prozent (n=1) Antworten auf die Klassen 3, 2 und 1 an (Abbildungen 10—12). Die Gesamtrate des Ansprechens auf die Kombinationstherapie von 308 nm monochromatischem Excimerlicht mit topischem Tacrolimus bei SV ist in Tabelle 2 dargestellt, während eine grafische Darstellung in Abbildung 13 dargestellt ist.













In der univariablen Analyse: Krankheitsdauer von sechs Monaten oder weniger (OR: 4,80, 95% -KI: 1,36—16,78; p=0,01), Enddosis von 300 bis 900 mJ (OR: 4,90, 95% -KI: 1,49—16,28; p=0,01), Abschluss von 20 oder weniger Behandlungssitzungen (OR:8,50, 95% -KI: 1,42—49,40; p=0,02), durchschnittliche Energie von weniger als 400 mJ (OR: 16,78, 95% CI: 2,05—137, p=0,01) und Gesicht und Taille als häufigste Stelle von Vitiligo (OR: 188,67, 95% -KI: 3,13—11.271,13; p=0,01 für Gesicht und OR:105,64, 95% -KI: 1,55—7.269,01; p=0,03 für die Taille) waren statistisch signifikante Kovariaten, die negativ mit dem Erfolg der Kombinationstherapie assoziiert waren (Tabelle 3).
Während der multivariablen Analyse, Enddosis von 300 bis 900 mJ (OR: 15,96, 95% -KI: 1,72—148,41; p=0,02) und Taille oder Leistengegend als Ort der Vitiligo (OR: 237,46, 95% -KI: 1,73—32.869,62;p=0,03 für Taille und OR: 0,11, 95% CI: 0,00—22,87; p=0,02 für die Leistengegend) wurden als unabhängige Faktoren identifiziert, die mit der Wirksamkeit der Kombinationstherapie in Verbindung stehen (Tabelle 3).
Die altersbasierte Analyse ergab, dass die Erfolgsrate bei Vitiligo im Kindesalter (d. h. bei Auftreten in einem Alter unter 12 Jahren) bei 80,95 Prozent lag (n=17/21), wohingegen die Erfolgsrate bei erwachsenen Patienten (d. h. in einem Alter von über 12 Jahren) bei 75 Prozent lag (n=18/24).
Von 45 Patienten traten bei neun (20%) Nebenwirkungen im Zusammenhang mit der Kombinationstherapie auf, während bei 36 (80%) Patienten keine Beschwerden auftraten. Von den neun Patienten, bei denen Komplikationen auftraten, wurde bei drei (33,3%) Patienten ein Erythem beobachtet, bei zwei (22,2%) Patienten eine Verkrustung, bei einem (11,1%) Patienten eine periläsionale Hyperpigmentierung, bei einem (11,1%) Patienten eine Blasenbildung und bei einem (11,1%) Patienten eine postinflammatorische Hyperpigmentierung.
Diskussion
Ein Excimer-Laser verwendet die Kombination aus einem Edelgas (z. B. Argon, Krypton oder Xenon) und einem reaktiven Gas (z. B. Fluor oder Chlor). Ein Excimer (d. h. ein angeregtes Dimer) ist ein kurzlebiges Molekül, das aus zwei Spezies besteht, von denen sich mindestens eine in einem elektronisch angeregten Zustand befindet. Diatomische Komplexe, an denen ein Edelgas und ein Halogenid wie Xenonchlorid beteiligt sind, sind bei der Konstruktion von Excimer-Lasern üblich.10 Unter geeigneten Bedingungen von elektrischer Stimulation und hohem Druck entsteht ein Pseudomolekül, ein sogenanntes Excimer, das nur in einem energetisierten Zustand existieren kann und bei seiner Rückkehr in den Grundzustand Energie in Form von ultraviolettem Licht freisetzt.11 Definitionsgemäß sind die Atome eines Excimermoleküls zwei oder mehr Atome desselben chemischen Elements. Bei Atomen verschiedener Elemente (z. B. Xenonchlorid) wird das Phänomen als „Exziplex“ bezeichnet.12
Der Xenonchlorid-Excimer-Laser oder MEL emittiert monochromatische Strahlung mit einer Wellenlänge von 308 nm. MEL unterscheidet sich vom Laser dadurch, dass das emittierte Licht inkohärent und nicht kollimiert ist. Es weist jedoch immer noch das medizinisch relevante Merkmal der Monochromatizität auf, das für die Behandlung von Vitiligo erforderlich ist. MEL hat sich als erythemogener erwiesen als ein Excimer-Laser.10
Excimer-Laser und MEL haben ähnliche Wirkmechanismen. Die Wellenlänge von 308 nm wirkt sich auf die Kern-DNA aus, die als Chromophor wirkt, was den DNA-Bruch erleichtert und zu einer Verringerung der T-Zell-Proliferation führt.13 Dies reguliert auch das Tumorsuppressorgen p53 hoch und verursacht dadurch Zellzyklusarrest und Apoptose.14 Abgesehen von diesen immunologischen Wirkungen wird auch angenommen, dass es aufgrund eines Anstiegs der Peptidendothelin-1-Inkeratinozyten zur Migration und Proliferation von Melanozyten führt.15
MEL hat gegenüber Excimer-Lasern gewisse Vorteile, wie zum Beispiel die Kosten. Excimer-Laser sind mit wiederkehrenden Kosten verbunden, die durch den Austausch potenziell toxischer Gase verursacht werden. Bei MEL ist das aktive Medium, Xenonchlorid, hermetisch in einer Glasröhre versiegelt und muss nicht gewechselt werden. Der Laser hat im Verhältnis zum Licht eine kleinere Spotgröße. Aufgrund von Hochspannungsentladungen und der Entsorgung potenziell giftiger Gase wirft dies auch eine Reihe von Sicherheitsproblemen auf. Darüber hinaus hat MEL mehrere Vorteile gegenüber der herkömmlichen Schmalband-UV-B-Therapie, die langsam wirkt, viel Bürofläche benötigt und in pädiatrischen Fällen schwierig anzuwenden ist. Da die Behandlung mit MEL verhindert, dass normale Haut in Kontakt kommt, können supraerythemogene Dosen angewendet werden. Die Methode nimmt weniger Platz ein und die Behandlung ist relativ schneller.
MEL ist der Schmalband-Ultraviolett-B-Phototherapie bei der Induktion der T-Zell-Apoptose überlegen.16 Le Duff u.a.10 und Qiong Shi u.a.17 zeigte eine ähnliche Wirksamkeit von Excimer-Laser und MEL bei der Behandlung von Vitiligo. Casacci et al.18 berichtete, dass die Excimer-Lampe wirksamer war als das schmalbandige Ultraviolett-B-Licht.
Topischer Tacrolimus ist ein ausgezeichneter Immunmodulator. Es reguliert verschiedene proinflammatorische Zytokine wie Interleukin (IL) -2, IL-3, IL-4, IL-5, Interferon-C, den Tumornekrosefaktor Alpha und granulozytenstimulierende Faktoren herunter. Es fördert die Proliferation und Migration von Melanozyten.9,19
Tacrolimus-Salbe als Monotherapie führt bei SV-Patienten zu einem variablen, aber unbefriedigenden Ansprechen.20 Verschiedene Studien haben jedoch die Wirksamkeit einer Kombinationsbehandlung mit Tacrolimus und Excimer-Laser oder -Lampe bei Vitiligo gezeigt.8,21
SV ist eine Art von Vitiligo, die durch depigmentierte Makula oder Flecken gekennzeichnet ist, die in einer gemusterten Verteilung angeordnet sind. Es macht 5 bis 27,9 Prozent der untersuchten Fälle von Vitiligo aus.22,23 Es macht 30 Prozent der Fälle von Vitiligo im Kindesalter aus.24 Eine indische Studie ergab eine Prävalenz von 6,7 Prozent bei Patienten mit Vitiligo in Indien.25 Es setzt früh in der Kindheit ein. Die Läsionen entwickeln sich innerhalb kurzer Zeit in einem lokalisierten Bereich schnell und bleiben dann stabil. Das Verteilungsmuster der Läsionen kann dermatomal, blaschkoid, phylloid oder schachbrettartig sein.26,27 Für die Ätiopathogenese von SV wurden mehrere Hypothesen vorgeschlagen, darunter neuronaler Mechanismus, somatischer Mosaikismus, mikrovaskuläres Skin-Homing und eine kombinierte Drei-Stufen-Theorie.28 Autoimmunität und Familienanamnese treten bei SV seltener auf.29,30 Es spricht schlecht auf eine medizinische Behandlung an. Wenn die Läsionen jedoch früh nach Beginn der Behandlung behandelt werden, scheinen sie empfindlicher auf die Therapie zu reagieren.31 In einer Studie wurde berichtet, dass ein potentes topisches Kortikosteroid bei 34,2 Prozent der Patienten eine Repigmentierung von über 50 Prozent hervorruft.32 Eine chirurgische Therapie allein oder in Kombination mit einer adjuvanten medizinischen Behandlung führt bei SV häufig zu einer zufriedenstellenden Reaktion.33,34
In der vorliegenden Studie mit 45 Patienten mit SV waren die weiblichen Patienten zahlreicher als die männlichen Patienten. Dies könnte auf einen größeren Behandlungswunsch weiblicher Patienten aufgrund sozialer Stigmatisierung zurückzuführen sein.
Die Reaktion auf die Phototherapie, entweder mit PUVA,35 311-nm-Schmalband-Ultraviolett B,36 oder der Excimer-Laser ist bei Patienten mit SV schlechter als bei Patienten mit Nicht-SV.5 Eine retrospektive Studie von Bae Jung et al.6 berichteten bei 50 Prozent ihrer Patienten von einer Repigmentierung von mehr als 75 Prozent.6 Sie verwendeten eine Kombination aus Behandlungen, einschließlich Excimer-Laser, topischem Tacrolimus und einer kurzen oralen Behandlung mit Steroiden. In der vorliegenden Studie wiesen 16 (35,6%) Patienten eine vollständige Repigmentierung auf, und 19 (42,2%) Patienten wiesen eine Repigmentierung von 75 bis 99 Prozent auf. Das allgemeine Ansprechen auf die Behandlung lag bei 77,8 Prozent, wobei nur ein Patient keine Repigmentierung zeigte. Im vorliegenden Studienprotokoll wurden keine systemischen Steroide verwendet.

Die Krankheitsdauer war ein statistisch signifikanter Faktor für das Ergebnis einer SV-Erkrankung. Die Krankheitsdauer korrelierte negativ mit dem Behandlungserfolg.28 Bae Jung u.a.6 berichtete, dass eine Krankheitsdauer von mehr als 12 Monaten ein unabhängiger prognostischer Faktor für den Krankheitsverlauf war. In unserer Studie wirkte sich eine Krankheitsdauer von mehr als sechs Monaten negativ auf die Erfolgsrate aus. Der Ort der Erkrankung ist ebenfalls ein wichtiger Faktor für das Behandlungsergebnis.37 Patienten mit Gesichtsläsionen sprechen im Vergleich zu Patienten mit akralen Läsionen schneller auf die Behandlung an. Die vorliegende Studie ergab, dass Gesichtsläsionen und Läsionen an der Taille signifikant besser auf die Behandlung ansprachen. Das unterschiedliche Ansprechen an verschiedenen Läsionsstellen könnte durch die Dauer der Erkrankung beeinflusst werden, da Patienten mit Gesichtsläsionen in der Regel früher zur Behandlung kamen als Patienten mit Läsionen an anderen Stellen. Kinder sprachen besser auf die Behandlung an als Erwachsene, der Unterschied war jedoch statistisch nicht signifikant. Die endgültige Dosis von MEL und die Anzahl der Behandlungssitzungen standen in der vorliegenden Studie in umgekehrter Beziehung zur Ansprechrate. Das Verfahren wurde ohne signifikante Nebenwirkungen gut vertragen. Leichte Nebenwirkungen wie Erythem und periläsionale Hyperpigmentierung wurden festgestellt und klangen ohne Intervention ab. Keiner der Patienten brach die Studie aufgrund seiner Nebenwirkungen ab. Die Einschränkungen unserer Studie waren die geringe Stichprobengröße und das Fehlen einer Kontrollgruppe.
Fazit
SV spricht schlecht auf die Behandlung an und macht chirurgische Modalitäten zur Hauptstütze der Behandlung. Aufgrund bestimmter operativer Komplikationen und der Schwierigkeiten bei der Durchführung von Eingriffen bei Kindern wurde in dieser Studie eine MEL mit 308 nm untersucht. Es ist kostengünstiger, schneller, kompakter in der Anwendung und sicherer. Es zielt nur auf die betroffenen Läsionen ab. Da Kombinationstherapien bei Vitiligo am besten wirken, wurden eine 308-nm-Excimer-Lampe und der topische Immunmodulator 0,1% Tacrolimus kombiniert. Diese Kombination erwies sich als wirksam und sicher, wenn sie zu einem frühen Zeitpunkt im Krankheitsverlauf begonnen wurde.
Referenzen
- Taïeb A, Picardo M. Clinical practice. Vitiligo. N Engl JMed. 2009; 360(2):160–169.
- Alikhan A, Felsten LM, Daly M, et al. Vitiligo: a comprehensive overview Part I. Introduction, epidemiology, quality of life, diagnosis, differential diagnosis, associations, histopathology, etiology, and work-up. J Am Acad Dermatol. 2011;65(3):473–491.
- Lee DY, Kin CR, Park JH, et al. The incidence of leukotrichia in segmental vitiligo: implication of poor response to medical treatment. Int J Dermatol.2011;50(8):925–927.
- Lee DY, Park JH, Lee JH, et al. Surgical treatment is indicated in long-duration segmental vitiligo. Dermatol Surg. 2010;36(4):568–569.
- Do JE, Shin JY, Kim DY, et al. The effect of 308nm excimer laser on segmental vitiligo: a retrospective study of 80 patients with segmental vitiligo. Photodermatol Photoimmunol Photomed.2011;27(3):147–151.
- Bae JM, Yoo HJ,Kim H, et al. Combination therapy with 308-nm excimer laser, topical tacrolimus, and short-term systemic corticosteroids for segmental vitiligo: a retrospective study of 159 patients. J Am Acad Dermatol. 2015;73(1):76–82.
- Passeron T, Ortonne JP. Use of the 308-nm excimer laser for psoriasis and vitiligo. Clin Dermatol. 2006;24(1):33–42.
- Li L, Liang Y,Hong J, et al. The effectiveness of topical therapy combined with 308-nm excimer laser on vitiligo compared to excimer laser monotherapy in pediatric patients. Pediatr Dermatol. 2019;36(1):e53–e55.
- Lan CC, Chen GS, Chiou MH,et al. FK506 promotes melanocyte and melanoblast growth and creates a favourable milieu for cell migration via keratinocytes: possible mechanisms of how tacrolimus ointment induces repigmentation in patients with vitiligo. BrJ Dermatol. 2005;153(3):498–505.
- Le Duff F, Fontas E, Giacchero D, et al. 308-nm excimer lamp vs. 308-nm excimer laser for treating vitiligo: a randomized study. Br J Dermatol. 2010;163(1):188–192.
- Park KK, Liao W,Murase JE. A review of monochromatic excimer light in vitiligo. Br JDermatol. 2012;167(3):468–478.
- Spencer JM, HadiSM. The excimer lasers. J Drugs Dermatol. 2004;3(5):522–525.
- Beggs S, Short J,Rengifo-Pardo M, Ehrlich A. Applications of the excimer laser: a review. DermatolSurg. 2015;41(11):1201–1211.
- Bulat V, SitumM, Deiol I, et al. The mechanisms of action of phototherapy in the treatment of the most common dermatoses. Coll Antropol. 2011;35(Suppl 2):147–151.
- Pacifico A,Leone G. Photo(chemo)therapy for vitiligo. Photodermatol Photoimmunol Photomed. 2011;27(5):261–277.
- Ozawa M, Ferenczi K,Kikuchi T et al. 312-nanometer ultraviolet B light (narrow-band UVB) induces apoptosis of T cells within psoriatic lesions. J Exp Med. 1999;189(4):711–718.
- Shi Q, Li K, Fu J, etal. Comparison of the 308-nm excimer laser with the 308-nm excimer lamp in the treatment of vitiligo—a randomized bilateral comparison study. Photodermatol Photoimmunol Photomed. 2013;29(1):27–33.
- Casacci M, Thomas P,Pacifico A, et al. Comparison between 308 nm monochromatic excimer light and narrowband UVB phototherapy (311–313 nm) in the treatment of vitiligo—a multicentre controlled study. J Eur Acad Dermatol Venereol. 2007;21(7):956–963.
- Jung H, Oh ES. FK506positively regulates the migratory potential of melanocyte-derived cells by enhancing syndecan-2 expression. Pigment Cell Melanoma Res. 2016;29(4):434–443.
- Kathuria S, KhaitanBK, Ramam M, Sharma VK. Segmental vitiligo: a randomized controlled trial to evaluate efficacy and safety of 0.1% tacrolimus ointment vs 0.05% fluticasone propionate cream. Indian J Dermatol Venereol Leprol. 2012;78(1):68–73.
- Wu Y, Sun Y, Qiu L,et al. A multi-centre, randomized, split-face and/or neck comparison of 308-nm excimer laser and 0.1% tacrolimus ointment for stable vitiligo, plus intramuscular slow-releasing betamethasone for active vitiligo. Br JDermatol. 2019;181(1):210–211.
- el-Mofty AM, el-MoftyM. Vitiligo A symptom complex. Int J Dermatol. 1980;19(5):237–244.
- Koga M, Tango T.Clinical features and course of type A and type B vitiligo. Br J Dermatol. 1988;118(2):223–228.
- Hann SK, Lee HJ.Segmental vitiligo: clinical findings in 208 patients. J Am Acad Dermatol. 1996;35(5 Pt 1):671–674.
- Khaitan BK, PasrichaJS, Sood A. clinical profile of 450 Indian vitiligo patients. American Academyof Dermatology 61st Annual Meeting; March 21–26, 2003; San Francisco, CA.
- van Geel N, Bosma S,Boone B, et al. Classification of segmental vitiligo on the trunk. Br JDermatol. 2014;170(2):322–327.
- Kim DY, Oh SH, HannSK. Classification of segmental vitiligo on the face: clues for prognosis. BrJ Dermatol. 2011;164(5):1004–1009.
- van Geel N, Speeckaert R. Segmental vitiligo. Dermatol Clin. 2017;35(2):145–150.
- Khaitan BK, KathuriaS, Ramam M. A descriptive study to characterize segmental vitiligo. Indian JDermatol Venereol Leprol. 2012;78(6):715–721.
- Ezzedine K, Diallo A,Léauté-Labrèze C, et al. Multivariate analysis of factors associated with early-onset segmental and nonsegmental vitiligo: a prospective observational study of 213 patients. Br J Dermatol. 2011;165(1):44–49.
- ParkJH, Park SW, Lee DY, et al. The effectiveness of early treatment in segmental vitiligo: retrospective study according to disease duration. Photodermatol Photoimmunol Photomed. 2013;29(2):103–105
- Khalid M, Mujtaba G.Response of segmental vitiligo to 0.05% clobetasol propionate cream. Int JDermatol. 1998;37(9):705–708 .
- Lee DY, Park JH, LeeJH, et al. Surgical treatment is indicated in long-duration segmental vitiligo. Dermatol Surg. 2010;36(4):568–569.
- Mulekar SV. Along-term follow-up study of segmental and focal vitiligo treated by autologous, non-cultured melanocyte keratinocyte cell transplantation. ArchDermatol. 2004;140(10):1211– 1215.
- Tallab T, Joharji H,Bahamdan K, et al. Response of vitiligo to PUVA therapy in Saudi patients. IntJ Dermatol. 2005;44(7):556–558.
- Anbar TS, WesterhofW, Abdel-Rahman AT, El- Khayyat MA. Evaluation of the effects of NB-UVB in bothsegmental and non-segmental vitiligo affecting different body sites. Photodermatol Photoimmunol Photomed. 2006;22(3):157–163.
- Cho S, Zheng Z, ParkYK, Roh MR. The 308-nm excimer laser: a promising device for the treatment of childhood vitiligo. Photodermatol Photoimmunol Photomed. 2011;27(1):24–29.
